퇴행성 뇌질환 (Neurodegenerative disease)
정상적인 사람이 나이가 들면서 세포가 손상되어 점차 증세가 나타나는 것.
흔함 정도: 알츠하이머>파킨슨>루게릭
루게릭병Lou Gehrig[amyotrophic lateral sclerosis(ALS)]
운동 신경세포(Motor neuron)의 퇴화(Degeneration)에 의해 근육의 약화(Weakness)와 함께 자발적 움직임(Voluntary movement)이 소실되는 질환.
대뇌 겉질(피질)의 위운동신경세포(upper motor neuron, 상위운동신경세포)와 뇌줄기(뇌간)/ 척수의 아래운동신경세포(lower motor neuron) 모두가 점차적으로 파괴
임상 증상은 서서히 진행되는 사지의 위약(weakness, 쇠약) 및 위축으로 시작하고, 병이 진행되면서 결국 호흡근 마비로 수년 내에 사망.
Risk factor
일 년에 10만 명당 약 1~2명에게서 루게릭병이 발병하는 것으로 알려져 있다.
남성이 여성에 비해 1.4~2.5배 정도 더 발병률이 높다.
주로 50~70대의 중장년층 및 노인층에서 나타나며, 약 10%의 환자에게 가족력이 있다.
이 중 약 20%의 가족에서 21번 염색체에서 원인 유전자의 돌연변이가 확인되고 있다.
현재까지 모두 8곳의 유전자가 가족성 루게릭병을 유발한다.
그 외는 산발성(sporadic)으로 인해 발병한다.
고엽제, defoliant
원인
정확히 밝혀지지 않았습니다.
원인유전자
가장 잘 알려진 변이는 과산화물제거효소(Superoxide dismutase, SOD) 유전자이다.
과산화물제거효소는 세포내의 대사과정에서 생성되는 과산화기(Superoxide radical, O2-)를 다시 산소(Oxygen)으로 변환하는 역할을 한다.
과산화물제거효소 유전자 변이 -> 정상적인 기능X ->과산화기가 세포 내에 축적->세포의 사멸(Death)
15개 정도의 원인유전자( 세포 내의 매우 다양한 기능에 관여)
EX) RNA에 결합하는 단백질, 세포내 소포 운송(Vesicle trafficking)에 관여하는 단백질, 세포 분영(Cell division)에 관여하는 단백질
발병기전
흥분독성(Excitotoxicity): 알파 운동 신경세포(Alpha motor neuron)의 퇴화가 주로 관여하며, 운동 신경세포의 퇴화를 유발하는 구체적 기전으로 관여
글루탐산(Glutamate) 등의 신경전달물질(Neurotransmitter)이 너무 많이 분비되거나, 이에 대한 수용체(Receptor)가 너무 많이 활성화되었을 때, 신경세포가 손상되거나 죽는 현상.
치매(Alzheimer's disease) 등의 다양한 퇴행성뇌질환(Neurodegenerative disease)의 원인.
환자의 뇌척수액(Cerebrospinal fluid)에서 글루탐산의 양이 많으며, 신경세포의 시냅스(Synapse)에서 글루탐산의 재흡수에 관여하는 글루탐산 수송체(Glutamate transporter)에 이상.
-> 시냅스에서 글루탐산이 높은 농도로 계속 유지되어 흥분독성이 유발됨.
증상
사지의 근력 약화(weakness, 쇠약) (한 부위에서 여러군대로 퍼짐)
근 위축
사지 마비
언어 장애
호흡 기능의 저하
호흡기기(respiratory regulator) 이용 페렴으로 사망
위운동신경세포가 파괴되면서 겉질숨뇌로와 겉질척수로가 점차 손상->이에 따라 뇌줄기, 목, 가슴, 허리엉치분절이 담당하는 얼굴, 몸통, 사지에 상위운동신경upper motor neuron손상적 증상(근육의 경련(cramp)& 경직(spasticity))가 나타난다.
근육의 경련(cramp)& 경직(spasticity)
또한 척수의 각 분절의 앞뿔에 위치한 아래운동신경세포가 파괴되면서 아래운동신경세포(하위운동신경lower motor neuron손상적 증상(다발수축증(fasciculation) ))가 함께 나타난다
삼킴곤란(dysphagia) & 사래(aspiration)
호흡곤란(exertional dyspnea)
호흡부전(respiratory failure)
허나 방광 및 장조절(bowel/bladder control), 의식, 외안근(extraocular muscle) 및 성적기능엔 영항X
진단 diagnosis
일차적- 임상적 증상.
전기생리학적 검사, 조직병리학적 검사,혈액검사,신경전도 검사
뇌척수액 검사(요추 천자), 근조직 생검,뇌-척수 X-ray 및 MRI, 유전자 검사, 근전도 검사(EMG)(다른질병과 비교)
치료
릴루졸(Riluzole):흥분독성& 글루탐산 기전에 근거하여 글루탐산(glutamate) 방출을 억제하는 약물인 릴루졸(Riluzole)/최초의 치료제.
줄기세포치료제 뉴로나타
비타민 E로 예방
파킨슨병Parkinson’s disease
정의
뇌간(정확히는 중뇌)에 위치한 흑질에서 도파민을 분비하는 신경세포가 원인 모르게 서서히 소실되어 가는 질환
주로 진전(tremor), 근육의 강직(rigidity), 안정시 떨림,자세 불안정(굽은자세), 몸 동작이 느려지는 서동(bradykinesia) 등의 운동 장애가 나타나는 질환.
파킨슨병의 증상은 뇌흑질 치밀부의 도파민계 신경이 60~80% 정도 소실된 후에 명확하게 나타납니다.
병리 검사를 시행하면 뇌와 말초신경의 여러 부위에 발병성 알파시누클레인 단백질이 침착되어 생긴 루이소체를 확인할 수 있습니다.
파킨슨 증후군은 신경퇴행성 질환들과 2차성 질환으로 나뉜다.
신경퇴행성 질환들은 주로 이상 단백(dysprotein)이 신경세포에 쌓여서 신경세포가 괴사하여 발생,
ex) 파킨슨병, 진행성 핵상마비, 다계통 위축증, 루이소체 치매, 피질기저하 변성
이 때문에 파킨슨병 외에 다른 종류들을 비전형적 파킨슨 증후군(Atypical Parkinsonism, 또는 Parkinson Plus Syndrome)이라고 부른다
2차성 파킨슨 증후군은 이상 단백의 침착이 아닌 다른 이유로 파킨슨 증상이 생기는 경우를 가리킨다.
여기에는 뇌졸중, 일산화탄소 중독, 일본뇌염, 약물 중독, 외상 등이 포함된다.
파킨슨 증상을 야기하는 약물들로는 신경이완제(neuroleptic)인 chlorpromazine, haloperidol, perphenazine 등이 있으며, 그 외 metoclopraide 와 resperpine이 있다.
다만 뇌졸중의 경우 뇌졸중이 한 번 생겼다고 파킨슨 증상을 보이는 예는 적으며, 보통 여러 번 반복된 다음에 발생한다.
또 뇌졸중이 생긴 바로 다음에는 파킨슨 증상이 없다가 시간이 꽤 경과한 다음에 생기는 경우가 많다.
원인(risk factor)
발생빈도는 인구 1,000 명 당 1명 내지 2명
파킨슨병은 주로 노년층(65<)에서 발생하는 질환
남성에게 더 흔함
가족력 있음
한국인들은 파킨슨병 발병 유전자를 가지고 있다.(LRRK2 G2385R)
유전적 파킨슨병보다는 특발성 파킨슨병의 빈도가 훨씬 높음
Exogenous factor: 독소(pesticide, rotenone), 바이러스, 외상(trauma)
Endogenous factor: endogenous toxin
1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine(MPTP), 살충제(로테논, 파라콰트), 중금속(망간, 납, 구리), 일산화탄소, 유기 용매, 미량 금속 원소 등의 독소 노출, 두부 손상
원인
뇌의 신경전달물질 중의 하나인 도파민(dopamine)의 결핍으로 인해 유발되며, 병리소견으로 흑색질의 도파민 신경세포의 소멸 및 루이소체의 침착이 관찰.
환자의 90% 내지 95%를 점유하는 '산발적 파킨슨병(sporadic PD)'이, 뉴런에 생긴 미토콘드리아 폐기물의 처리(diposal waste)를 제어하는 신호 이상에서 비롯됨.
이 경로가 막히면 미토콘드리아 손상 폐기물이 과도히 쌓여 뉴런이 사멸하고 파킨슨병으로 이어졌다.
어떤 신체 부위에 감염이 생기면 확산을 막기 위해 싸우지만, 감염이 제거되면 여기에 관여한 신호도 사라져야 한다.
그런데 파킨슨병 환자는 1형 인터페론 경로를 여닫는 PICS2라는 단백질의 신호 조절이 잘 안됨.
정상 작동하는 1형 인터페론 경로는 바이러스 퇴치에 중요한 역할을 하지만, 뇌 신경세포의 에너지 공급에도 깊숙이 관여.
파킨슨병의 문제는 PIAS2 단백질이 필요하지 않을 때도 1형 인터페론 경로를 봉쇄하는 데 있었다.
감염 상황이 종료되면 이 경로의 봉쇄가 풀려 정상으로 돌아가야 하는데 파킨슨병 환자는 그렇지 않았다.
증상(50~70%이상의 흑색질(Substantia Nigra)파괴시)
1) 주요 증상
① 진전(tremor at rest): 안정시 마치 손으로 알약을 빚거나 동전을 세는 듯한 모습의 진전(pill-rolling tremor)을 보임
② 서동(bradykinesia/hypokinesia/akinesia): 보행, 얼굴표정, 말하기 등 몸의 움직임이 느려지는 것으로 증상은 다음과 같다. 보폭이 작아지고 발이 지면에서 많이 떨어지지 않으며 발을 끌면서 걷고, 보행시 팔의 흔들림이 작아지다가 점차 팔이 흔들림 없이 굽혀져 몸 옆에 붙은 상태로 보행하는 것이 특징이다. 환자가 보행시 앞으로 쓰러지는 경향을 보일 수도 있다. 파킨슨병 환자들은 표정이 점차 없어져 마치 가면을 쓴 것 같다고 해서 가면안(masked face)이라고 불리는 얼굴 모양을 한다. 음량이 점차 작아지고 웅얼거리게 되며 억양과 리듬감도 단조로워지고 발음장애도 동반된다.
③ 강직(rigidity): 근육이 뻣뻣해지는 것을 말한다. 환자의 팔을 굽힐 때 마치 납으로 만든 파이프를 굽히는 것 같고, 천천히 굽혀 보면 톱니바퀴를 돌리는 것처럼 규칙적으로 저항감이 오는 cogwheel rigidity를 보인다.
④ 자세불안정(postural instability): 파킨슨병이 진행되면 자세의 불안정이 나타나고, 병이 진행되면 이로 인해 자꾸 넘어지게 된다.
렘 수면 장애(REM sleep behavior disorder)
(2) 운동기능과 관련되지 않은 증상
① 자율신경계 이상: 배뇨장애 및 변비, 성기능이상, 체위성 저혈압, 기타 자율신경이상
② 감각이상: 주로 팔다리, 허리, 목 근육의 통증을 호소하는데, 파킨슨병의 운동증상과 밀접한 관계가 있을 것으로 생각된다. 적절한 약물치료로 운동장애가 호전되면 통증도 같이 감소하는 경우가 많다.
③ 정신기능이상: 사고의 속도가 다소 느려지고, 경미한 기억장애나 주의집중장애가 나타나며, 이해력과 논리적인 사고력이 떨어질 수 있다. 정서적인 장애는 비교적 흔히 관찰되며 우울증과 불안증이 자주 동반된다.
자율신경계 증상(기립성 저혈압, 소변장애, 성기능 장애),
위장관 장애(침 흘림, 삼킴 장애, 변비),
인지기능 장애(경도 인지 장애, 치매),
우울, 불안, 충동 조절 장애,
정신과적 증상(환각, 망상),
수면장애(렘수면 장애, 불면증, 낮 동안의 졸림),
통증, 피로, 후각 장애
삼킴곤란(dysphagia), 구음장애(dysarthria)
(3) 치료약 투약 관련 증상
① Dyskinesia
② Motor fluctuation
③ Cognitive and behavioral disturbances
④ Orthostatic hypotension
진단
초기 증상으로 판별하기 힘듬
증상으로 판별해야 하며 밑의 것들은 보조적임
파킨슨병의 진단에는 전문의의 병력청취와 신경학적 검사가 가장 중요합니다.
MRI나 CT등의 기타 검사 (다른 질병과의 혼동을 피하기 위해)
단일광전자방출단층촬영(SPECT), 양전자방출단층촬영(PET)
치료
(1) 약물치료
① 레보도파(L-dopa) 제제: DDC inhibitor인 carbidopa나 benserazide와의 복합제를 사용한다.-5년정도 후 효과 줄어듬
・ Sinement®: L-dopa+carbidopa
・ Madopar®: L-dopa+benserazide
② 도파민 수용체 작용제: bromocriptine, pergolide, ropinirole, pramipexole
③ 분해효소억제제
・ MAOB 억제제: selegiline
・ COMT 억제제: entacapone, tolcapone
④ 항콜린 약제
⑤ NMDA 길항제
⑥ 기타: 비전형적 항정신병제제(Clozapine)
(2) 수술적 치료
① 정위수술법(stereotaxic surgery): 시상절제술(thalamotomy), 창백핵절단술(pallidotomy)
② 심부뇌자극술(deep brain stimulation)
③ Neural transplantation: fetal tissue graft, 줄기세포(stem cell), 유전자치료(gene therapy)
제 3세계에서 마리화나 등을 처방 한다고 함
알츠하이머병Alzheimer's disease


정상 알츠하이머
치매(전체의 60%)를 일으키는 가장 흔한 퇴행성 뇌질환.
알츠하이머병은 이상 단백질(아밀로이드 베타 단백질, 타우 단백질)이 뇌 속에 쌓이면서 뇌 신경세포가 서서히 죽어감
여기서 퇴행성이란 정상적인 사람이 나이가 들면서 세포가 손상되어 점차 증세가 나타나는 것을 말합니다.
전체 치매 환자의 50~60% 정도가 알츠하이머병에 의한 치매 증상을 보이는 것으로 알려져 있습니다. .
그 진행과정에서 인지기능 저하뿐만 아니라 성격변화, 초조행동, 우울증, 망상, 환각, 공격성 증가, 수면 장애 등의 정신행동 증상이 흔히 동반되며 말기에 이르면 경직, 보행 이상 등의 신경학적 장애 또는 대소변 실금, 감염, 욕창 등 신체적인 합병증까지 나타나고 결국에는 모든 일상 생활 기능을 상실. .
알츠하이머병 환자의 뇌 조직을 검사시 특징적인 병변인 신경반(neuritic plaque)과 신경섬유다발(neurofibrillary tangle) 등이 관찰
육안 관찰 시에는 신경세포 소실로 인해 전반적 뇌 위축 소견이 보인다.
->질병 초기에는 주로 기억력을 담당하는 주요 뇌 부위인 해마와 내후각뇌피질 부위에 국한되어 나타나지만 점차 두정엽, 전두엽 등을 거쳐 뇌 전체로 퍼져나간다.
[65세> 조발성(초로기presenility)(유전적요인) 알츠하이머/65세< 만발성(노년기) 알츠하이머]
조발성 알츠하이머병은 비교적 진행 속도가 빠르고 언어기능의 저하가 비교적 초기에 나타남
만발성 알츠하이머병의 경우 상대적으로 진행이 느리고 다른 인지기능 저하에 비해 기억력의 손상
*두 연령 구분에 따른 병리 소견의 차이는 없음, 동일 질병으로 간주.
알츠하이머병의 경우 뇌세포는 점차 퇴화되고 비정상 단백질이 뇌에 축적되어 뇌 크기가 줄어들면서 정신기능이 떨어져 치매가 된다.
아세틸콜린 저하가 특징
risk factor
연령 : 65세 이상에서 발병률이 높다./80세 이상의 여성
유전 : 가족 간에 유전되는 경우가 있다. 다운증후군(유전적인 요인이 전체 알츠하이머병 발병의 약 40~50%).
생활습관 : 위험 요인은 원인에 따라 달라진다.
성별 : 여성
낮은 학력, 우울증 병력이나 두부 손상의 과거력
고혈압, 당뇨, 고지질혈증, 비만
원인
(유전적 질병은 젊은 사람에게4~50대/40~50%)
21번 염색체에 이상이 있는 '다운 증후군'(몽고증) 환자는 중년기가 되면 거의 대부분 알츠하이머병과 같은 뇌의 변화가 나타납니다.
21번 염색체에 있는 아밀로이드 전구단백질(APP) 유전자에 돌연변이가 있으면 65세 이전에 치매가 나타나며, 이를 조발성 가족성 알츠하이머병이라고 합니다.
이외에도 14번 염색체에 있는 PS1(프리세닐린 1 유전자) 유전자의 돌연변이, 1번 염색체에 있는 PS(프리세닐린)2 유전자의 돌연변이도 가족성 알츠하이머병을 유발합니다.
19번 염색체에는 아포지단백 E ε4(APOE ε4) 유전자가 있습니다(대표적).
( 1개 가지고 있을 경우 약 2.7배, 2개 가지고 있는 경우 17.4배 정도 알츠하이머병의 위험성이 높아짐)
아포지질단백은 지질을 운반하는 단백질인데, 피 속의 콜레스테롤 조절 및 지질대사에 관여합니다.
여기에는 E2, E3, E4의 세 가지 대립유전자가 있습니다.
그중에서 E4 대립유전자가 가족성 알츠하이머병과 65세 이후에 산발적으로 생기는 만발성 치매의 위험 인자로 작용합니다.
또한 신경 전달 물질의 경로, 특히 콜린 계통의 이상도 알츠하이머병에 영향을 미칩니다.
X단일질환,신경계 노화 현상이 진행되는 상태에서 유전적 위험 요소와 환경적 위험 인자가 더해져 복합적인 발병 기전에 의해 나타나는 증후군으로 볼 수 있습니다.
기전

베타 아밀로이드(beta-amyloid)라는 작은 단백질이 과도하게 만들어져 뇌에 침착되면서 뇌 세포에 유해한 영향을 주는 것이 메인 발병의 핵심 기전
그 외 뇌 세포의 골격 유지에 중요한 역할을 하는 타우 단백질(tau protein)의 과인산화, 염증반응, 산화적 손상 등도 뇌 세포 손상에 기여하여 발병에 영향을 미침.
대표적인 뇌 병리 소견인 신경반(혹은 노인반)은 베타 아밀로이드 단백질의 침착과 관련되며, 신경섬유다발은 타우 단백질 과인산화와 연관이 있다.
증상
1. 기억력 감퇴
기억력감퇴는 알츠하이머병의 초기부터 가장 흔하게 나타나는 증상이다. 최근의 대화내용을 반복적으로 묻게 되고, 약속을 잊는 일이 잦아지며, 최근에 있었던 일이나 사건을 기억하지 못하는 등의 증상이 나타나게 된다. 좀 더 진행하면 사람 만난 일을 잊거나 식사를 하고 난 지 얼마 되지 않아 밥을 찾기도 하며 금방 들었던 말도 곧 잊어버리게 된다. 초기에는 자신의 신상에 관한 정보(가족 이름, 주소, 태어난 곳, 출신 학교, 직업 등)나 오래된 과거에 대한 기억은 비교적 잘 유지되는데, 병이 진행하면 점차 이마저도 잊게 된다.
2. 언어능력 저하
초기에는 말을 하려 할 때 적절한 단어가 떠오르지 않아 ‘그것, 저것’ 등의 대명사로 표현하거나, 말을 주저하고 말문이 막히는 ‘단어 찾기 곤란’ 증상이 나타난다. 이때는 말을 비교적 유창하게 할 수 있어 주변에서 언어장애가 있다는 것을 잘 느끼지 못한다. 그러나 병이 점차 진행하면서 점차 말로 표현하는 것이 어려워지고 말수도 줄게 되며, 상대방의 말을 잘 이해하지 못하게 된다.
3. 시공간파악능력(지남력)의 저하
시간이나 장소, 사람을 알아보는 능력을 지남력이라고 한다. 초기에는 시간 지남력이 저하되어 날짜나 요일을 모르는 증상이 나타나고 점차 중요한 기념일이나 집안 대소사 날을 챙기지 못하게 된다. 더욱 심해지면 연도나 계절을 파악하지 못하고 낮과 밤을 혼동해 새벽에 일어나 밥을 하는 등의 모습을 보이기도 한다. 시간 지남력보다 좀 늦게 장소에 대한 지남력 저하가 나타나는데 처음에는 익숙하지 않은 장소에서 혼동을 보이다가 진행되면 늘 다니던 익숙한 곳에서 길을 잃어 헤매는 일도 생긴다.
그러다가 결국에는 자신이 있는 곳이 어디인지 전혀 알지 못하게 된다. 사람에 대한 지남력 장애는 가장 늦게 나타나는데 먼 친지부터 시작해서 진행하면 늘 함께 지내는 자녀나 배우자를 알아보지 못하게 되기도 한다.
4. 판단력 및 일상생활수행능력의 저하
병이 진행하면서 추상적으로 사고하고, 문제를 해결하며, 적절한 결정이나 판단을 내리는 능력이 저하된다. 따라서 일을 계획하거나 결정하며 제대로 수행해 나가는 것이 어려워지기 때문에 큰돈을 관리하거나, 여행 또는 사교모임, 직업 활동 등을 하기가 어렵게 된다. 더 진행하면 간단한 돈 계산, 간단한 집안일, 가전제품 사용, 취미활동 등 익숙하게 해오던 일을 처리하지 못하게 되고 결국에는 식사하기, 대소변가리기, 몸치장하기, 위생관리 등 가장 기본적인 일상활동들도 스스로 수행하지 못하게 된다.
5. 정신행동증상
인지기능장애 이외에도 성격변화, 초조행동, 우울증, 망상, 환각, 공격성 증가, 수면장애, 무감동 및 무관심 등 이른바 ‘정신행동증상’이 흔하게 동반된다. 본래의 성격과 다르게 의욕이 없고 사람들과 어울리지 않고 집에만 있거나, 반대로 사소한 일에도 짜증, 화, 공격적인 말이나 행동을 보인다(성격변화). 남들이 물건을 훔쳐가고 자신을 해치려 한다는 등의 의심과 피해의식에 사로잡히기도 하고(망상), 헛것을 보거나 듣기도 한다(환각).
주변을 배회하거나 안절부절 못하고 초조해하며 왔다 갔다 하기도 하고, 도움을 완강히 거부하고 공격적인 행동을 하기도 한다(초조행동). 그 밖에 불면과 같은 수면장애도 흔하며, 저녁이 되면서 혼돈이 심해지는 일몰증후군(sundowning)이 나타나기도 한다.
6. 신체 증상
알츠하이머병이 상당히 진행되면 대소변 실금이 나타나고, 몸이 경직되고 보행장애가 나타나 거동이 힘들어진다. 거동 장애와 더불어 욕창, 폐렴, 요도감염, 낙상 등의 신체적 문제가 합병증으로 나타나기가 쉽다.
7. 행동 증상, 정신증적 증상
행동 증상은 환자의 가족들을 곤란하게 만드는 증상입니다. 주로 도둑 망상과 부정 망상이 흔하게 나타납니다. 텔레비전에서 나오는 인물과 대화하려고 하거나, 거울에 비친 자신을 인식하지 못하고 대화하려는 증상이 생길 수 있습니다. 주로 알츠하이머병이 악화된 중기 이후에 보입니다. 주위의 물건과 사람들을 잘못 인식합니다. 초조, 불안, 공격성 증가 등으로 보호자나 간병인의 부담이 심해져서, 환자를 의료 시설에 입원시켜야 할 수 있습니다.
10. 야간 착란
진단/검사
보호자를 통한 정확한 병력 청취 중요.
인지 기능의 변화가 있는지, 있다면 언제부터 어떠한 양상으로 나타났는지 확인
1. 신체검사와 신경학적 검사
환자의 인지 기능에 영향을 줄 수 있는 신체질환 및 뇌신경계 질환의 징후가 있는지 진찰.
현미경으로 알츠하이머병 환자의 뇌 조직을 검사하였을 때 특징적인 병변인 신경반(neuritic plaque)과 신경섬유다발(neurofibrillary tangle) 등이 관찰된다.
육안 관찰 시에는 신경세포 소실로 인해 전반적 뇌 위축 소견이 보인다. 이러한 뇌 병리 소견은 질병 초기에는 주로 기억력을 담당하는 주요 뇌 부위인 해마와 내후각뇌피질 부위에 국한되어 나타나지만 점차 두정엽, 전두엽 등을 거쳐 뇌 전체로 퍼져나간다.
2. 정신상태 검사
기억력 등의 인지기능을 평가하고 섬망이나 혼돈과 같은 의식의 장애가 있는지, 우울증이나 망상, 환각 등의 동반된 정신행동증상이 있는지를 평가.
3. 일상생활동작 검사
일상생활에서의 기능수준이 어느 정도인지를 평가.(식사, 옷 입기, 씻기, 대소변 가리기 등의 기본적인 일상생활/ 전화하기, 음식물 만들기, 돈 관리하기 등 좀 더 복잡한 일상생활동작)
4. 혈액 검사 등의 실험실 검사
치매 상태를 초래할 수 있는 여러 신체질환을 파악하기 위해 빈혈검사, 간기능검사, 신기능검사, 당뇨검사, 비타민검사, 갑상선기능검사, 지질검사, 흉부 X레이, 심전도, 소변검사 등 다양한 실험실 검사를 시행한다.
5. 뇌 영상검사
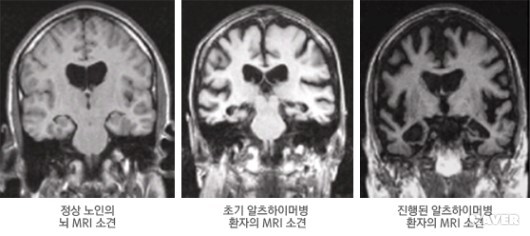
알츠하이머병 MRI 영상
MRI,CT등 구조적 뇌 영상검사/
뇌의 위축, 뇌실 확대 등 뇌의 구조적 이상 소견을 확인할 수 있다.
최근 CT보다 해상도가 높은 MRI를 널리 사용.
MRI 검사상 특징적인 내측두엽 위축 소견이 비교적 초기 단계에서부터 확인됨.
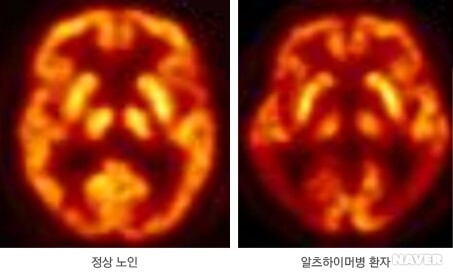
양자방출단층촬영(PET), 단일광자방출촬영(SPECT) 등 기능적 뇌 영상검사.
PET이나 SPECT와 같은 기능적 뇌 영상검사를 시행하면 뇌의 혈류량 또는 뇌의 포도당 대사능력 등을 측정함으로써 뇌 각 부위의 기능 이상을 확인할 수 있다.
구조적 뇌 영상검사에서 별다른 이상이 나타나지 않는 초기 알츠하이머병의 경우에도 기능적 뇌 영상검사로 뇌 기능의 저하 여부와 저하 부위(측두엽 및 두정엽 대사 저하)를 조기에 확인할 수 있어 조기 진단에 매우 유용.
검사 정확도에 있어 PET이 SPECT보다 우수하여 기능적 뇌 영상검사가 필요한 경우 PET 사용이 권고.
최근 알츠하이머병의 핵심 병리인 아밀로이드 판 등 베타아밀로이드 단백질 응집 상태 자체를 영상화 할 수 있는 리간드들도 개발되어 사용되고 있다.
대표적인 아밀로이드 PET 영상 리간드로 11C-Pittsburg Compound B(PIB)가 있다.
6. 신경심리검사
뇌 기능과 관련된 다양한 인지기능을 객관적으로 정밀하게 평가하는 검사이다.
기억력, 언어능력, 주의집중력, 판단능력, 계산능력, 수행능력, 시공간파악능력 등 다양한 인지영역에 대한 광범위한 평가가 포함.
결과를 통해 어떤 영역의 인지기능이 어느 정도 수준으로 저하되었는지에 대한 객관적 정보를 얻을 수 있으며, 이러한 정보는 치매 여부의 진단이나 원인 감별에 참고자료로 활용된다.
또한 치료 시작 전 신경심리검사를 통해 환자의 기저 인지기능 수준에 대한 정보를 미리 얻어 둠으로써 향후 치료 효과 파악을 위한 기준으로 활용할 수 있다.
치료
아세틸콜린 분해효소 억제제(6개월~2년정도 진행을 늦춤)경증~중증
아세틸콜린 (신경전달물질)의 양을 증가시킴으로써 작용하며 뇌손상이 심하지 않은 경도 및 중등도 환자에 보다 효과적
NMDA(N-methyl-D-aspartate) 수용체 길항제antagonism중증이상
비약물적 치료
영역을 훈련시키거나, 손상되지 않은 인지 영역을 극대화하여 손상된 인지영역을 보완해주는 기억력 훈련, 인지재활치료, 현실 지남력 훈련
서울대학교병원 의학정보, 서울대학교병원
'++ 건강 동맥·성' 카테고리의 다른 글
| 서동증, 진전, 근육강직 (1) | 2023.03.15 |
|---|---|
| 본태성 진전증(떨림) 발생단계 1. 소뇌 기능 저하 2. 기저핵 기능이상 3. 시상 기능이상 4. 뇌흑질 퇴화 (2) | 2023.03.15 |
| 파킨슨이 주로 손떨림이나 보행장애같이 운동영역에 영향을 미친다고 알고 있는바와 다르게 사실 빈 운동 영역 영향 또한 크다. 우울증, 기억상실뿐만 아니라 후각 상실, 수면장애, 인지장애,.. (0) | 2023.03.14 |
| 강털소나무(bristlecone pine) 4,900년까지 된 개체도 있다 (0) | 2022.02.24 |
| 노화의 종말 책 하버드 의대 수명 혁명 프로젝트 / 노화는 질병이며, 치료 가능하다. (0) | 2022.02.24 |